|
| ¿De qué está hecho el Universo? |
Chicos:
Versión 3.4
Última modificación: 2023-03-05
El Universo que habitamos está hecho de materia y energía. Antiguamente creíamos que toda la materia del Universo era igual a la materia que conocemos (la que constituye nuestros cuerpos y los objetos que nos rodean).
Sin embargo, aunque la Materia Oscura fue propuesta hace 90 años por Fritz Zwicky, fue hace unos 45 que se asentó el consenso de que la Materia Oscura existe y es mayoritaria en el Universo (1).
La materia oscura, sabemos que existe, pero no de qué está hecha. Así que la ignoraremos y estudiaremos solamente la materia común, misma que nos conforma y nos rodea en lo inmediato. La materia común está conformada por Moléculas (mol- = masa y -ulas = pequeñas) y éstas a su vez de átomos.
Las sustancias de Materia común de nuestro Mundo suelen encontrarse mezcladas, separarlas es difícil y generalmente el éxito en obtenerlas en estado puro es relativo. Siempre quedan algunas otras sustancias que denominamos impurezas (im- = negación, pur- = puro y -eza = propiedad o cualidad).
 |
| ¿Cuál porcentaje constituye la materia común del Universo? |
La materia oscura, sabemos que existe, pero no de qué está hecha. Así que la ignoraremos y estudiaremos solamente la materia común, misma que nos conforma y nos rodea en lo inmediato. La materia común está conformada por Moléculas (mol- = masa y -ulas = pequeñas) y éstas a su vez de átomos.
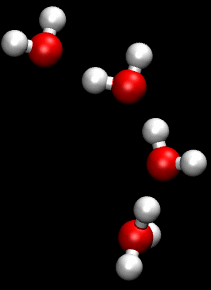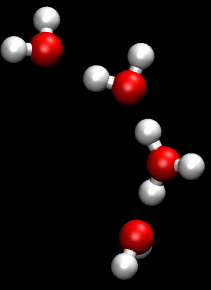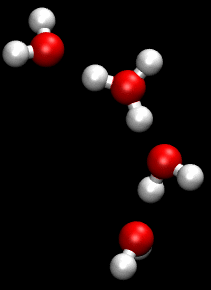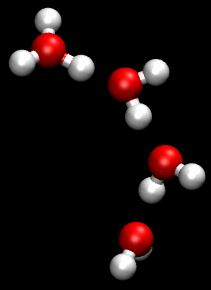 |
| 4 moléculas de agua. |
Las sustancias de Materia común de nuestro Mundo suelen encontrarse mezcladas, separarlas es difícil y generalmente el éxito en obtenerlas en estado puro es relativo. Siempre quedan algunas otras sustancias que denominamos impurezas (im- = negación, pur- = puro y -eza = propiedad o cualidad).
Antes de plantear como separarles estudiaremos a las sustancias y sus propiedades en las siguientes diapositivas:
En el siguiente video describe las mismas diapositivas de la presentación de arriba:
(1) J Einasto, E Saar, Ants Kaasik & AD. Chernin 1974 Missing mass around galaxies: morphological evidence Nature 252, 111-3
CG 2. Para que extiendan sus competencias de apreciación artística: